Antecedentes:
El cribado neonatal se utiliza para la detección precoz de trastornos metabólicos y endocrinos congénitos que, si no se tratan, pueden provocar crisis mortales o daños a largo plazo. En Alemania, el cribado de recién nacidos está regulado en la guía para niños del Comité Conjunto Federal (G-BA). Los informes de calidad son creados y publicados anualmente por la Sociedad Alemana de Cribado Neonatal (Informe DGNS). Los datos de los informes de la DGNS 2006-2018 son la base de este trabajo.
Método:
Para los años 2006-2018, se calcularon las prevalencias y se evaluaron los datos sobre la calidad del proceso.
Resultado:
Entre 9,218,538 nacimientos, 6,917 recién nacidos fueron identificados con una enfermedad objetivo. La prevalencia general es de 75 por 100 000 recién nacidos, siendo el hipotiroidismo congénito el más común con 30 por 100 000, seguido de fenilcetonuria (PKU) y deficiencia de acil-CoA deshidrogenasa de cadena media (MCAD) con 10 por 100 000 cada uno. De las 272.205 revisiones solicitadas, se recibió el 80%. La tasa de resultados positivos de detección (recuperación) cayó del 0,90 % en 2006 al 0,37 % en 2018. Cada quinto resultado positivo de detección confirmó una enfermedad objetivo. El tratamiento se inició en el 79% de los niños con indicación de terapia dentro de las dos semanas.
Conclusión:
La baja tasa de recuperación y el inicio temprano del tratamiento en el 79 % de los niños afectados hablan de la eficacia del programa. La integración de estructuras de seguimiento y la introducción de un registro podrían mejorar aún más la calidad del programa.
El cribado neonatal de trastornos metabólicos y endocrinos congénitos es una de las medidas de prevención secundaria más exitosas en la infancia. Los recién nacidos han sido examinados para detectar fenilcetonuria (PKU) desde finales de la década de 1960 y, desde la década de 1980, también para detectar hipotiroidismo y galactosemia. En 2004, el Comité Conjunto Federal (G-BA) incluyó el llamado "cribado extendido del recién nacido" (ENS) para doce enfermedades diana en la guía pediátrica y, por tanto, en la atención estándar y añadió la tirosinemia tipo I en 2018 y la combinada grave en 2019 Inmunodeficiencias (SCID) (1). La detección de la fibrosis quística se introdujo en 2016 con regulaciones separadas (2).
Algunas enfermedades específicas pueden provocar crisis metabólicas potencialmente mortales o daños permanentes en una etapa temprana. En consecuencia, el objetivo de la ENS es identificar la mayor cantidad de niños afectados lo antes posible, pero al mismo tiempo alarmar solo a unas pocas familias de niños sanos con un resultado falso positivo (conspicuo) (3). Esto requiere un proceso estandarizado con responsabilidades definidas; este proceso se especifica en las guías de información y consentimiento de los niños, implementación y contenido del tamizaje y servicios de laboratorio (1, 2). Sin embargo, el registro de diagnósticos de confirmación, la evaluación de la detección y el seguimiento no están regulados. Este último está destinado a garantizar que se verifiquen los hallazgos notorios o los hallazgos que deben repetirse.
Métodos
El proveedor de servicios responsable del nacimiento del niño es responsable de realizar la evaluación del recién nacido. Antes de la extracción de sangre, los padres deben ser informados sobre el cribado neonatal, normalmente por un médico, de acuerdo con las especificaciones de la Ley de Diagnóstico Genético (4) y dar su consentimiento por escrito. La sangre nativa debe tomarse entre las 36 y las 72 horas de vida, gotear sobre un papel de filtro especial, secarse y enviarse a un laboratorio de detección. Si el niño es dado de alta antes de las 36 horas de vida, se debe realizar un cribado precoz en el centro de maternidad. Para estos niños y para los bebés prematuros, de quienes la primera muestra se tomó antes de las 32 semanas de gestación (SG), es obligatorio un control a las 36 horas de vida oa las 32 semanas de gestación.
Un resultado de detección positivo (recuperación) representa un diagnóstico sospechoso y debe aclararse más de inmediato. Dependiendo de la gravedad del hallazgo positivo y de la sospecha diagnóstica, se recomienda repetir el tamizaje o aclaración directa (diagnóstico de confirmación) en un centro especializado.
De acuerdo con las directrices para niños, los laboratorios deben presentar un informe de calidad todos los años, que se publica para todos los laboratorios de detección alemanes como un informe de detección nacional de la Sociedad Alemana de Detección de Recién Nacidos e. V. (DGNS) y publicado en www.screening-dgns.de/reports.php (5). Los laboratorios notifican datos acumulados sobre la calidad del proceso y datos individuales seudonimizados sobre diagnósticos de confirmación a la DGNS. Se comprueba la plausibilidad de los datos y los casos se validan utilizando criterios definidos. Los casos validados positivamente y los casos sin información sobre el diagnóstico de confirmación, en los que los valores de detección repetidos ("detección clara del recién nacido") hablan con una probabilidad muy alta de la exactitud del diagnóstico sospechoso, están relacionados con los nacimientos informados en Alemania para el cálculo de la prevalencia.
Los datos de los informes DGNS 2006-2018 (5) se usaron y procesaron para esta publicación. Los datos de cribado de fibrosis quística solo están disponibles a partir de 2016. Se publicarán por separado, ya que aquí se utiliza un algoritmo de detección complejo, cuya presentación y los problemas resultantes irían más allá del alcance de esta publicación. La evaluación estadística se realizó con SPSS 25.
Resultados
En Alemania, once laboratorios están autorizados actualmente para proporcionar y facturar exámenes de detección de recién nacidos. En Baviera, también se incluye un centro de detección que es independiente de los laboratorios en la Oficina Estatal de Salud y Seguridad Alimentaria de Baviera para garantizar una alta calidad del proceso y evaluar la detección (6, 7, 8, 9) (eBox 1). A menos que se indique lo contrario, todos los datos y cálculos de esta publicación se refieren al período completo de 2006 a 2018.
caja
Parámetros de calidad en el cribado neonatal
Ampliar imagenTodas las imágenes
Cuadro electrónico 1
Organización estructural del cribado neonatal alemán
Ampliar imagenTodas las imágenes
Totales
En un cribado poblacional, el éxito depende esencialmente de una alta tasa de participación, que se logró con 9.244.411 exámenes de cribado documentados en 9.218.538 nacimientos (10) en Alemania. El mayor número de exámenes se puede explicar, entre otras cosas, por muestras de niños no registrados en Alemania. Se documentaron un total de 8.471 negativas de toda la ENS (1 de cada 1.000 recién nacidos).
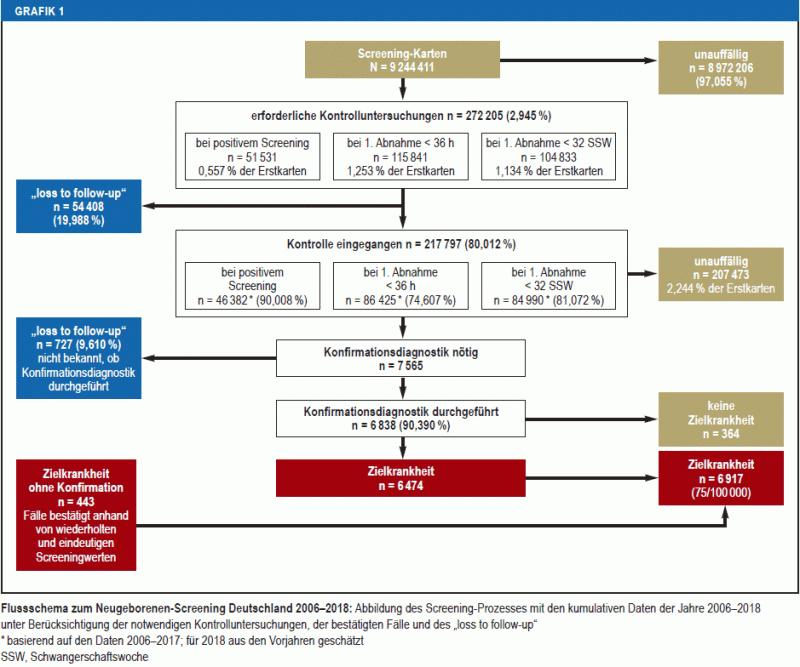
Los laboratorios solicitaron exámenes de seguimiento (tarjetas duplicadas) para 30 niños de 1000 (n=272 205); la mayoría debido a una extracción de sangre antes de las 36 horas de vida (13 de 1000; n = 115 841) o antes de las 32 semanas de gestación (11 de 1000; n = 104 833). Se requirió seguimiento después de un resultado positivo de tamizaje (recall) en 51.531 recién nacidos (6 de 1.000) y se realizó en el 90,01% de los niños. Se realizaron el 80,01% (n = 217.797) de las revisiones solicitadas (Figura 1).
Gráfico 1
Diagrama de flujo para el cribado neonatal Alemania 2006-2018
Ampliar imagenTodas las imágenes
Tiempos de proceso
Los tiempos de proceso cortos son decisivos para la efectividad del tamizaje neonatal para lograr el tratamiento más temprano posible de los niños afectados (3). La extracción de sangre antes de las 72 horas de vida tiene un aporte significativo y se realizó en el 96,22% de los recién nacidos en 2018 (eFigura 1, eRecuadro 2). Este es un aumento del 13,85 % con respecto a 2006. Por el contrario, la proporción de muestras de sangre con más de dos días entre la recolección y la recepción en el laboratorio aumentó del 42,08 % en 2006 al 51,64 % en 2018 (eFiguras 2 y 3).
eGráfico 1
Edad en la extracción de sangre 2006-2018
Ampliar imagenTodas las imágenes
eGráfico 2
Tiempo desde la extracción de sangre hasta la recepción en el laboratorio
Ampliar imagenTodas las imágenes
eGráfico 3
Lapso de tiempo desde la recepción del laboratorio hasta la notificación de los resultados
Ampliar imagenTodas las imágenes
Cuadro electrónico 2
Evolución de los tiempos de proceso 2006-2018 en lo que respecta al diagnóstico precoz
Ampliar imagenTodas las imágenes
6.014 de los 6.917 niños con diagnóstico confirmado requirieron tratamiento, que se inició dentro de la primera semana de vida para 3.127 recién nacidos (51,95%) y en la segunda semana de vida para otros 1.627 niños (27,05%). Esto significa que el 79,05% de los recién nacidos afectados fueron tratados dentro de las dos semanas posteriores al nacimiento (mediana de inicio de la terapia = 7 días de vida). 778 niños fueron tratados posteriormente, incluidos 342 (43,96%) niños con hipotiroidismo, 124 (15,94%) con deficiencia de acil-CoA deshidrogenasa de cadena media (MCAD) y 145 (18, 64%) con deficiencia de biotinidasa (parcialmente parcial). La proporción de niños que iniciaron tardíamente el tratamiento se mantiene constante a lo largo de los años, al igual que la proporción de niños cuyo inicio de tratamiento se desconoce (n = 482; 8,02%). En 901 niños con hiperfenilalaninemia leve, no hubo indicación de terapia; dos bebés muy prematuros fallecieron antes del inicio de la terapia (eFigura 4).
eGráfico 4
Edad al inicio de la terapia
Ampliar imagenTodas las imágenes
Prevalencia
La prevalencia de enfermedades congénitas raras depende de la composición étnica de la población de cribado y solo puede calcularse de forma válida cuando el número de casos es alto. En el presente conjunto de datos, se documentó una enfermedad diana para 6.917 recién nacidos, es decir, para 75 de cada 100.000 (Tabla 1).
Tabla 1
Enfermedades objetivo en el cribado neonatal alemán 2006-2018; Comparación de prevalencia con estimaciones de 2004
Ampliar imagenTodas las imágenes
En 37 niños con resultados de detección normales (falsos negativos), se diagnosticó una enfermedad objetivo según los síntomas clínicos y los hallazgos se informaron al laboratorio de detección (8 niños con síndrome adrenogenital, 29 niños con hipotiroidismo). Estos son informes individuales, ya que no existe un registro en Alemania en el que se documenten todos los casos de enfermedad.
Calidad analítica
La calidad de un procedimiento de prueba (recuadro) se determina utilizando la sensibilidad, la especificidad y el valor predictivo positivo (VPP). El PPV describe la probabilidad con la que se confirmará el diagnóstico si el resultado del tamizaje es positivo y depende de la tasa de recuerdo (tasa de resultados positivos del tamizaje) y la prevalencia. La tasa de recuperación mejoró a lo largo de los años del 0,90% al 0,37%, con una variación significativa entre enfermedades (Tabla 2, Gráfico 2). Actualmente (datos de 2018), se pueden esperar 370 resultados positivos de 100.000 exámenes de detección, de los cuales 78 están confirmados (PPV = 21,1%). Esto significa que se confirma que uno de cada cinco niños con un resultado de detección positivo tiene la enfermedad; suele ser el caso de hallazgos altamente patológicos (91,434% confirmado en el diagnóstico de confirmación). No se puede calcular la sensibilidad porque no se registra sistemáticamente el número de niños perdidos en la evaluación.
Gráfico 2
Tasas de recuperación de enfermedades diana seleccionadas en el cribado neonatal alemán
Ampliar imagenTodas las imágenes
Tabla 2
Tasa de hallazgos patológicos de detección (tasa de recuperación) y valor predictivo positivo (VPP)
Ampliar imagenTodas las imágenes
"Pérdida durante el seguimiento"
De 272.205 revisiones solicitadas, incluidas 5.149 después de un resultado positivo de detección, 54.408 (19,99 %) no se realizaron ("pérdida de seguimiento"). No se dispone de datos diagnósticos de confirmación de otros 727 niños de los 7.565 recién nacidos (9,61%) con alto grado de sospecha de enfermedad diana (figura 1), incluido un tercio con sospecha de hipotiroidismo. En 443 de estos niños, los hallazgos del tamizaje también quedaron claros en la tarjeta de control, por lo que pudieron incluirse en el cálculo de la prevalencia. En 284 casos (3,75%) esto no fue posible.
En general, el 11,40 % de los 51 531 resultados positivos de las pruebas de detección no se aclararon o no estaban claros (Figura 1). Con un 1,14-37,28 % de información faltante en los diagnósticos de confirmación, existen grandes discrepancias entre los laboratorios.
Discusión
Por primera vez, el proceso de detección y los resultados de la "detección ampliada de recién nacidos" para toda Alemania de 13 cohortes de nacimiento con un total de 9,2 millones de niños se presentan en una sección longitudinal. Los resultados muestran que el tamizaje neonatal también se puede implementar con mucho éxito en una estructura federal con once laboratorios (eBox 1) si las responsabilidades y los procesos están claramente definidos. Se puede suponer que casi todos los recién nacidos son examinados, incluso si la comparación personal entre los niños nacidos y examinados solo se lleva a cabo en unas pocas regiones (3). Asimismo, la mitad de los niños afectados (mediana) pueden iniciar tratamiento precozmente a los siete días y el 79,05% a las dos semanas. Esto corresponde aproximadamente a los datos informados de Noruega (mediana = 6 días) y es significativamente anterior al 2012 para Europa por Burgard et al. (11) publicaron una mediana de 14,9 días y una aclaración del 75% de los resultados positivos del cribado en 20 días. Odenwald y colaboradores demostraron cuán importantes pueden ser el diagnóstico y la terapia precoces. para niños con síndrome adrenogenital (AGS). Si el tratamiento comenzó después de tres días, el 23,5% de los niños presentó un desequilibrio electrolítico, y si el tratamiento comenzó durante doce días o más, el 50% sufrió una crisis de pérdida de sal (desequilibrio electrolítico: 94,4%) (12). En el caso de otras enfermedades, el inicio precoz del tratamiento también puede ser determinante ante crisis o posibles secuelas a largo plazo (13, 14, 15). En general, ENS permite que la mayoría de los niños afectados se desarrollen normalmente gracias a la terapia temprana (13, 16, 17).
El efecto positivo de las reglamentaciones claras en los exámenes en serie se vuelve evidente cuando se consideran los componentes no reglamentados. Por un lado, no existen regulaciones sobre el seguimiento, por otro lado, los pacientes no se registran sistemáticamente para muchas enfermedades objetivo. Esto último es sin duda posible si se observa estrictamente la protección de datos, ya sea en los registros o mediante consultas sistemáticas en los centros de tratamiento, como se ha publicado para algunas enfermedades raras en Alemania (18, 19, 20, 21) y se requiere internacionalmente (22, 23, 24, 25, 26). Solo se pueden hacer afirmaciones válidas sobre la sensibilidad del cribado si se combinan los datos de todos los niños afectados. Se puede suponer un alto nivel de sensibilidad para las enfermedades metabólicas, ya que estas enfermedades raras suelen tratarse en unos pocos centros metabólicos. Aquí solo se informaron algunos resultados de detección falsos negativos. Esto es menos claro en el caso de las enfermedades endocrinas, ya que los niños con hipotiroidismo también son tratados en las consultas de los médicos generales. En principio, si existe sospecha clínica de alguna de las enfermedades diana, se debe realizar un diagnóstico específico aunque los hallazgos del cribado sean normales.
Para más de 55 000 niños, incluidos 5876 con un resultado positivo de detección, no está documentado si el resultado se verificó y aclaró alguna vez ("pérdida de seguimiento"). No se sabe si los padres no fueron informados o contactados por el remitente responsable del tamizaje o si no presentaron al recién nacido para el segundo análisis de sangre. Tampoco está claro con qué frecuencia no se aclaró más el resultado positivo o si el centro de tratamiento o el pediatra no informaron al laboratorio de detección del resultado del diagnóstico de confirmación. Para solucionar este problema es necesario un sistema de recordatorio estructurado, como se ha establecido en Bavaria, por ejemplo, con un centro de seguimiento desde 1999 (6, 7, 8, 9). En otros estados federales, el rastreo es realizado en parte por los laboratorios, pero sin financiamiento depende de los posibles recursos locales. Conocer los resultados de los diagnósticos de confirmación también es importante para el laboratorio para garantizar la calidad y optimizar el análisis.
La tasa de "pérdida de seguimiento" y el esfuerzo que implica el seguimiento continúan aumentando con cada nueva enfermedad objetivo incluida en el panel de detección. Hay una necesidad urgente de acción aquí. Al incluir el seguimiento en las pautas para niños y proporcionar la financiación adecuada, esta tarea podría transferirse a los laboratorios de detección además de a los centros independientes.
Un factor decisivo para la alta efectividad de la ENS es también la baja tasa de resultados positivos de detección (recordatorio), porque cada resultado falso positivo genera una preocupación innecesaria para las familias y costos en el sistema de atención médica. Mientras tanto, los criterios de calidad de la ENS, con una tasa de recuperación del 0,37 % (2018) y un VPP del 21 %, son muy superiores a los de otros métodos de cribado que también pueden calificarse de efectivos (mamografía de cribado: tasa de recuperación 3ª). -14 %, VPP 2-22 % [27]; cribado auditivo: tasa de recuerdo 5,3 %, VPP 6,2 % [28]). Sería posible una mejora adicional mediante el uso de métodos de análisis adicionales en un segundo paso de examen de la misma muestra de sangre en caso de un valor de detección anormal ("segundo nivel"), sin pasar por alto a los niños enfermos. Esto se muestra de manera impresionante en la detección de AGS (Figura 2) (29, 30) y es concebible para otras enfermedades. Sin embargo, esto aumenta el costo de la detección. En algunos países, como Noruega o Suecia, los análisis de segundo nivel también se usan para enfermedades metabólicas en el panel de detección (31, 32), en Alemania como parte de los estudios (33, 34).
Con la gran cantidad de aproximadamente 9,2 millones de niños examinados, la prevalencia de enfermedades congénitas raras para Alemania se puede calcular de manera válida, incluso si algunas prevalencias en los datos disponibles se deben a "pérdidas de seguimiento" y falta de retroalimentación de casos no detectados en el tamizaje podría estar subestimado. Las prevalencias no necesariamente pueden extrapolarse de otras poblaciones y en algunos casos muestran desviaciones significativas de los valores previamente adoptados y publicados sobre la base de números de casos mucho más pequeños y, a menudo, de otros países (Tabla 1) (16).
Base de datos
En este trabajo se presentan e interpretan los resultados más importantes de los informes de tamizaje 2006-2018 (5). Los informes elaborados por la DGNS corresponden en muchos aspectos a los criterios de calidad establecidos por Cornel et al. (24) y Ojodu et al. (35) se proponen o requieren para la evaluación de un programa de detección. Las limitaciones de estos datos son, por un lado, que no se dispone de resultados analíticos individuales y los datos del proceso solo se proporcionan de forma acumulativa; por otro lado, falta retroalimentación de los médicos tratantes sobre los diagnósticos de confirmación a los laboratorios, los cuales son requeridos para la validación de los casos sospechosos. Para estos últimos, sería de gran ayuda una normativa de obligado cumplimiento que tuviera en cuenta los requisitos de protección de datos de la Directiva sobre la infancia.
A diferencia de los informes organizados y financiados por el estado en los Países Bajos, Gran Bretaña y Noruega (32, 36, 37), el informe alemán fue creado por iniciativa de la sociedad especializada (DGNS) y los laboratorios y ha sido el único durante más de diez años Publicado el Informe de calidad sobre el cribado neonatal en Alemania (5). Con el fin de garantizar una alta calidad de la detección de recién nacidos y reconocer y comunicar rápidamente los desarrollos y tendencias, también con respecto a nuevas enfermedades objetivo, y para optimizar aún más la detección, se deben esforzar por obtener más regulaciones sobre evaluación y garantía de calidad en la guía para niños.
Conclusión
La detección de recién nacidos se está implementando en todo el país en Alemania con gran éxito y es un ejemplo impresionante de una medida preventiva eficaz en pediatría que se optimiza continuamente. En su conjunto, la proyección es un proceso complejo en el que intervienen diversos actores de distintos ámbitos. La garantía permanente de la alta calidad del tamizaje neonatal solo está garantizada si todos los componentes del tamizaje están sujetos a un proceso de mejora continua. Para ello es necesario el establecimiento de estructuras de seguimiento, un registro y aseguramiento continuo de la calidad, así como la evaluación de pruebas de cribado nuevas o modificadas.
Gracias
Nuestro agradecimiento especial al Prof. Dr. médico Heiko Krude y Erwin Lankes (Charité Berlin) por su apoyo en la validación de las enfermedades endocrinas y al Prof. Dr. médico Esther Maier (Dr. von Haunersches Children's Hospital LMU Munich) validando enfermedades metabólicas.
Contribuidores
Laboratorios de cribado Alemania:Dr. médico Oliver Blankenstein, Charité Newborn Screening Laboratory, Universitätsmedizin Berlin; Prof. Dr. re. por supuesto Uta Ceglarek, laboratorio de cribado de Leipzig, Instituto de Medicina de Laboratorio, Química Clínica y Diagnóstico Molecular (ILM), Hospital Universitario de Leipzig; dr. re. por supuesto Marina Stopsack, Instituto de Química Clínica y Medicina de Laboratorio, Hospital Universitario Carl Gustav Carus en la TU Dresden; Dr. PD médico Martin Lindner, Centro de Detección de Hesse, Hospital Universitario de Frankfurt; dr. re. por supuesto Cornelia Müller, Newborn Screening Center Mecklenburg-West Pomerania, University Medicine Greifswald; Prof. Dr. médico René Santer, laboratorio de cribado de Hamburgo, Hospital Infantil Universitario de Hamburgo; dr. médico dr. re. por supuesto Nils Janzen, Laboratorio de Cribado de Hannover; Prof. Dr. médico Gwendolyn Gramer, Heidelberg Newborn Screening, Hospital Universitario de Heidelberg; dr. médico Katrin Borucki, Instituto de Química Clínica y Patobioquímica, Hospital Universitario de Magdeburg; Dr. PD médico Wulf Röschinger, Laboratorio Becker & Colegas, tamizaje neonatal, Munich; dr. médico dr. re. por supuesto Hans-Wolfgang Schultis, laboratorio de detección, centro de atención médica SYNLAB en Weiden
Conflicto de intereses
Dra. Nennstiel ha recibido el reembolso de los gastos de viaje y de las conferencias de Biogen.
Los demás autores declaran no tener conflicto de intereses.
Datos del manuscrito
Enviado: 31/10/2019, versión revisada aceptada: 15/9/2020
Dirección de los autores
Dra. médico Uta Nennstiel, MPHBarea Estatal de Salud y Seguridad Alimentaria de VaraVeterinärstraße 2, 85764 OberschleißheimUta.Nennstiel@lgl.bayern.de
Estilo de cita
Lüders A, Blankenstein O, Brockow I, Ensenauer R, Lindner M, Schulze A, Nennstiel U, en nombre de los laboratorios de detección en Alemania: Detección neonatal de trastornos metabólicos y endocrinos congénitos: resultados de Alemania para los años 2006– 2018 Dtsch Ärzteebl Internacional 2021; 118:101-8.
DOI: 10.3238/arztebl.m2021.0009
►La versión en inglés del artículo está disponible en línea en: www.aerzteblatt-international.de
Material adicional
eGraphics, eBoxes: www.aerzteblatt.de/m2021.0009 o mediante código QR
1.Directrices del Comité Federal Conjunto sobre la Detección Temprana de Enfermedades en Niños (Directrices para Niños), 2020; Secciones 13-28. www.g-ba.de/downloads/62-492-2156/Kinder-RL_2020-05-14_iK-2020-03-25.pdf (último acceso el 15 de julio de 2020).
2.Directrices del Comité Federal Conjunto sobre la Detección Temprana de Enfermedades en Niños (Directrices para Niños), 2020; Secciones 29-42. www.g-ba.de/downloads/62-492-2156/Kinder-RL_2020-05-14_iK-2020-03-25.pdf (último acceso el 15 de julio de 2020).
3.Nennstiel-Ratzel U, Lüders A, Blankenstein O: Detección de recién nacidos: un excelente ejemplo de prevención secundaria eficaz. Gaceta Federal de Salud Investigación en Salud Protección de la Salud 2015; 58:139-45 Referencia cruzada MEDLINE
4.Ley de pruebas genéticas en humanos (Gene Diagnostics Act - GenDG), fecha de emisión 31/07/2009. www.gesetze-im-internet.de/gendg/BJNR252900009.html (último acceso el 15 de julio de 2020).
5.Nennstiel U, Lüders A, Blankenstein O, et al.: DGNS Screening Reports. www.screening-dgns.de/reports.php (último acceso el 15 de julio de 2020).
6.Nennstiel-Ratzel U, Liebl B, Zapf A: Proyecto modelo para la reorganización del cribado neonatal en Baviera. Salud 2003; 65: S31-5 Referencia cruzada MEDLINE
7.Liebl B, Nennstiel-Ratzel U, von Kries R, et al.: Detección ampliada de recién nacidos en Bavaria: seguimiento para lograr la repetición de la prueba solicitada. PrevMed 2002; 34:132-7 Referencia cruzada MEDLINE
8.Liebl B, Nennstiel-Ratzel U, von Kries R, et al.: Cumplimiento muy alto en un programa ampliado de detección de recién nacidos basado en EM-EM a pesar del consentimiento por escrito de los padres. PrevMed 2002; 34:127-31 Referencia cruzada MEDLINE
9.Liebl B, von Kries R, Nennstiel-Ratzel U, et al.: Aspectos éticos y legales del cribado neonatal. Carta mensual de medicina infantil 2001; 149:1326-35 Referencia cruzada
10Statistisches Bundesamt Deutschland – GENESIS-Online: Result 12612-0001 (destatis.de) (último acceso el 15 de julio de 2020).
11Burgard P, Rupp K, Lindner M, et al.: Programas de cribado neonatal en Europa; argumentos y esfuerzos en materia de armonización. Parte 2. Desde el cribado de los resultados del laboratorio hasta el tratamiento, el seguimiento y la garantía de calidad. J Inherit Metab Dis 2012; 35:613-25 Referencia cruzada MEDLINE
12Odenwald B, Dörr HG, Bonfig W, et al.: Hiperplasia suprarrenal congénita clásica debido a la deficiencia de 21-hidroxilasa: 13 años de detección y seguimiento neonatal en Bavaria. Klin Padiatr 2015; 227:278-83 Referencia cruzada MEDLINE
13Mütze U, Garbade S, Gramer G, et al.: Resultados a largo plazo de personas con enfermedades metabólicas identificadas a través de pruebas de detección en recién nacidos. Pediatría 2020; DOI: 10.1542/peds.2020-0444 (epub antes de la impresión) CrossRef MEDLINE
14Schweitzer-Krantz S: Diagnóstico temprano de trastornos metabólicos hereditarios para mejorar el resultado: el tema controvertido de la galactosemia. Eur J Pediatr 2003; 162: S50-3 Referencia cruzada MEDLINE
15.Leger J, Olivieri A, Donaldson M, et al.: Directrices de consenso de la Sociedad Europea de Endocrinología Pediátrica sobre detección, diagnóstico y tratamiento del hipotiroidismo congénito. Horm Res Pediatr 2014; 81: 80-103 Referencia cruzada MEDLINE
dieciséis.Schlune A, Riederer A, Mayatepek E, Ensenauer R: Aspectos del cribado neonatal en acidemia isovalérica. Cribado Neonatal Int J 2018; DOI: 10.3390/ijns4010007 Referencia cruzada MEDLINE PubMed Central
17Nennstiel-Ratzel U, Arenz S, Maier EM, et al.: Incidencia reducida de crisis metabólica grave o muerte en niños con deficiencia de acil-CoA deshidrogenasa de cadena media homocigotos para c.985A>Gidentificado por detección neonatal. Mol Genet Metab 2005; 85:157-9 Referencia cruzada MEDLINE
18El-Helou SM, Biegner AK, Bode S, et al.: El Registro Nacional Alemán de Inmunodeficiencias Primarias (2012-2017). Frente Immunol 2019; 10; DOI: 10.3389/fimmu.2019.01272 Referencia cruzada MEDLINE PubMed Central
19Nährlich L (ed.), Burkhard J, Wosniok J: German Cystic Fibrosis Register Report Volume 2018. www.muko.info/fileadmin/user_upload/angebote/qualitaetsmanagement/register/berichtsbaende/berichtsband_2018.pdf (último acceso el 15 julio de 2020).
20Ebrahimi-Fakhari D, Zemlin M, Sauer H, Poryo M, Graf N, Meyer S: Unidad de encuestas para enfermedades pediátricas raras en Alemania (ESPED) - 25 años de epidemiología pediátrica: un inventario. Klin Padiatr 2018; 230:215-24 Referencia cruzada MEDLINE
21Shai S, Perez-Becker R, Andres O, et al.: Incidencia de SCID en Alemania de 2014 a 2015. Una encuesta ESPED en nombre de la Unidad Alemana de Vigilancia Pediátrica API. J Clin Immunol 2020; 40:708-17 Referencia cruzada MEDLINE
22Hoffmann GF, Lindner M, Loeber JG: 50 años de cribado neonatal. J Inherit Metab Dis 2014; 37:163-4 Referencia cruzada MEDLINE
23Starkweather A, Coleman B, Barcelona de Mendoza V, et al.: Informe de política: mejorar la cobertura del cribado genético neonatal para incluir el Panel de cribado uniforme recomendado y el registro de cribado neonatal. Solo Outlook 2017; 65:480-4 Referencia cruzada MEDLINE PubMed Central
24Cornel MC, Rigter T, Weinreich SS, et al.: Un marco para iniciar el debate sobre las políticas de cribado neonatal en la UE: un documento de opinión de expertos. Eur J Hum Genet 2014; 22:12-7 CrossRef MEDLINE PubMed Central
25Kanungo S, Patel DR, Neelakantan M, Ryali B: Detección de recién nacidos y cambios en el rostro de los errores congénitos del metabolismo en los Estados Unidos. Ann Transl Med 2018; 6:468 CrossRefMEDLINE PubMed Central
26Lund AM, Hougaard DM, Simonsen H, et al.: Detección bioquímica de 504 049 recién nacidos en Dinamarca, las Islas Feroe y Groenlandia: experiencia y desarrollo de un programa de rutina para la detección ampliada de recién nacidos. Mol Genet Metab 2012; 107:281-93 Referencia cruzada MEDLINE
27Mandrik O, Zielonke N, Meheus F, et al.: Revisiones sistemáticas como "lentes de la evidencia": determinantes de los beneficios y daños de la detección del cáncer de mama. Int J Cáncer 2019; 145: 994-1006 Referencia cruzada MEDLINE PubMed Central
28Nennstiel U, Brockow I, Söhl K, et al.: Informe final sobre la evaluación del cribado auditivo neonatal 2011/2012, al 15 de enero de 2017. www.g-ba.de/downloads/17-98-4329/2017-05-18_Kinder-RL_Annahme_Endbericht_NHS-bericht.pdf (último acceso el 15 de julio de 2020).
29Janzen N, Sander S, Terhardt M, Peter M, Sander J: Cuantificación rápida y directa de esteroides suprarrenales mediante espectrometría de masas en tándem en suero y gotas de sangre seca. J Chromatogr B Analyt Technol Biomed Life Sci 2008; 861:117-22 Referencia cruzada MEDLINE
30Janzen N, Peter M, Sander S, et al.: Detección de hiperplasia suprarrenal congénita en recién nacidos: perfil de esteroides adicional mediante cromatografía líquida-espectrometría de masas en tándem. J Clin Endocrinol Metab 2007; 92:2581-9 Referencia cruzada MEDLINE
31Sörensen L, von Döbeln U, Ahlmann H, et al.: Detección ampliada de un millón de bebés suecos con R4S y CLIR para la evaluación posanalítica de los datos. Cribado Neonatal Int J 2020; 6:42 CrossRef PubMed Central
32.Tangeraas T, Sæves I, Klingenberg C, et al.: Rendimiento de la detección ampliada de recién nacidos en Noruega respaldado por herramientas bioinformáticas posanalíticas y análisis rápidos de ADN de segundo nivel. Cribado Neonatal Int J 2020; 6:51 Referencia cruzada MEDLINE PubMed Central
33.Röschinger W, Sonnenschein S, Schumann E, Nennstiel-Ratzel U, Roscher AA, Olgemöller B: Nuevas enfermedades diana en el cribado neonatal Recomendaciones de un proyecto piloto. Carta mensual para niños 2015; 2:142-9 Referencia cruzada
34.Gramer G, Hauk F, Lobitz S, Sommerburg O, Speckmann C, Hoffmann GF: Detección de recién nacidos 2020. Monatsschr Kinderheilkd 2017; 165:216-25 Referencia cruzada
35.Ojodu J, Singh S, Kellar-Guenther Y, et al.: NewSTEP: el establecimiento de un centro nacional de recursos de asistencia técnica para la detección de recién nacidos. Cribado Neonatal Int J 2018; 4:1 Referencia cruzada MEDLINE PubMed Central
36.van der Ploeg K, Wins S, Verkerk PH. La detección de manchas de sangre de recién nacidos en el monitor de los Países Bajos 2018. www.rivm.nl/sites/default/files/2020-01/HielprikMon2018-Engelstalig.pdf (último acceso el 15 de julio de 2020).
37.Begum F: Programa de detección de manchas de sangre en recién nacidos en el Reino Unido. Informe de análisis de rendimiento y recopilación de datos de 2016 a 2017. Publicado en mayo de 2018. https://assets.publishing.service.gov.uk/government/uploads/system/uploads/attachment_data/file/709367/Newborn_blood_spot_screening_data_collection_and_performance_analysis_report_2016_to_2017.pdf (último acceso el 15 de julio de 2020).
38.Lobitz S, Frömmel C, Brose A, Klein J, Blankenstein O: Incidencia de la enfermedad de células falciformes en una cohorte no seleccionada de recién nacidos nacidos en Berlín, Alemania. Eur J Hum Genet 2014; 22:1051-3 Referencia cruzada MEDLINE PubMed Central
39.Frömmel C, Brose A, Klein J, Blankenstein O, Lobitz S: Detección de anemia de células falciformes en recién nacidos: aspectos técnicos y legales de un estudio piloto alemán con 38 220 participantes. Biomed Res Int 2014; 2014: 695828 Referencia cruzada MEDLINE PubMed Central
40Vill K, Kölbel H, Schwartz O, et al.: Un año de detección de AME en recién nacidos: resultados de un proyecto piloto alemán. J Neuromuscul Dis 2019; 6:503-1 Referencia cruzada MEDLINE PubMed Central